全社會大關(guān)注、大參與、大投入帶來了高技術(shù)人才和高技術(shù)品種
利昂醫(yī)療表示在改革開放40年來,我國醫(yī)療器械產(chǎn)業(yè)在生產(chǎn)企業(yè)結(jié)構(gòu)、集聚區(qū)域、品種構(gòu)成、市場布局等方面都發(fā)生了巨大變化。
40年前,醫(yī)療器械產(chǎn)業(yè)缺乏自身技術(shù)特色,技術(shù)層次低,管理較為混亂。直至20世紀70年代末,原國家醫(yī)藥管理局組建,醫(yī)療器械產(chǎn)業(yè)才開始走上生產(chǎn)技術(shù)質(zhì)量集中統(tǒng)一管理的道路。特別是1986年,面對醫(yī)療器械產(chǎn)業(yè)混亂、產(chǎn)品落后的現(xiàn)狀,我國建立了由原航空工業(yè)部、原電子工業(yè)部、中國科學(xué)院、原衛(wèi)生部等部門領(lǐng)導(dǎo)組成的全國醫(yī)療器械協(xié)調(diào)聯(lián)席會議制度。1987年,國務(wù)院先后批轉(zhuǎn)原國家計劃委員會和原國家經(jīng)濟委員會下發(fā)的《關(guān)于加速發(fā)展醫(yī)療器械工業(yè)的請示》和《關(guān)于發(fā)展醫(yī)療器械工業(yè)若干問題的通知》,提出醫(yī)療器械產(chǎn)業(yè)的全社會統(tǒng)籌規(guī)劃和協(xié)調(diào)發(fā)展,打破系統(tǒng)和部門界限,為醫(yī)療器械大發(fā)展創(chuàng)造了良好的政策環(huán)境。不同門類的工業(yè)企業(yè)憑借自身的技術(shù)優(yōu)勢,紛紛投身開發(fā)與自身技術(shù)接近的醫(yī)療器械產(chǎn)品,醫(yī)療器械產(chǎn)業(yè)出現(xiàn)了全社會大關(guān)注、大參與、大投入的良好形勢。據(jù)1997年有關(guān)資料顯示,約有1800家軍工、機電、科研單位進入醫(yī)療器械產(chǎn)業(yè)。當時,產(chǎn)業(yè)中多種經(jīng)濟成分并存,其中,國有經(jīng)濟成分占百分之15,鄉(xiāng)鎮(zhèn)企業(yè)占百分之20,中外合資企業(yè)占百分之15,軍工機電系統(tǒng)占百分之50。
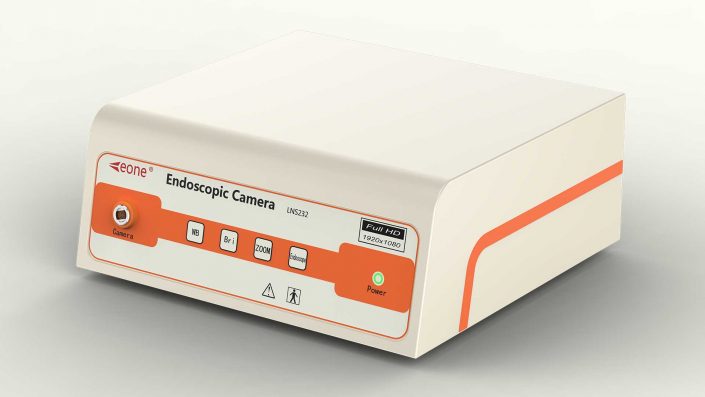
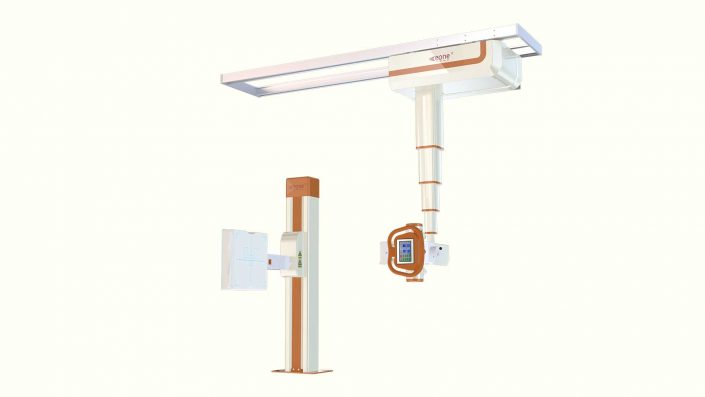
全社會大關(guān)注、大參與、大投入帶來了高技術(shù)人才和高技術(shù)品種,醫(yī)療器械如內(nèi)窺鏡攝像機等產(chǎn)業(yè)的發(fā)展狀況變好。醫(yī)療器械產(chǎn)業(yè)格局重新調(diào)整,新興的“長三角”“珠三角”和“環(huán)渤海”地區(qū)替代了原來長期處于上海、北京、天津的產(chǎn)業(yè)集聚區(qū),成為新的醫(yī)療器械產(chǎn)業(yè)集聚;產(chǎn)品種類不再局限于器械和衛(wèi)生材料制品,機電和智能化器械產(chǎn)品成為醫(yī)療器械的重要品種;開發(fā)研究機構(gòu)增多,一大批國家科研院所和大專院校積極參與醫(yī)療器械新產(chǎn)品的研發(fā)中,2000年我國對醫(yī)療器械科研開發(fā)的總投入已達到7400萬元。